成人动漫 王鹏飞团队一直致力于探索病毒感染、变异和免疫保护机制,围绕病毒免疫逃逸的防控瓶颈开展研究,在病毒对宿主和疫苗的免疫逃逸、抗病毒中和抗体及药物新靶点等方面取得了一系列重要学术成果。国际上率先报道新冠从早期Alpha、Beta到Omicron各种主要变异毒株对单克隆抗体和多克隆血清的免疫逃逸特征,鉴定出刺突蛋白上导致免疫逃逸的关键氨基酸突变位点,从分子层面揭示了这些毒株的免疫逃逸机制(Nature 2021, 593, 130–135,第一作者;Cell Host & Microbe 2022, 30(8):1077-1083.e4,Cell Discovery 2022, 8(1):110;Cell Discovery2023, 9(1):64,Cell Host & Microbe2024,32:25-34.e5,Signal Transduction and Targeted Therapy 2024;9(1):123,均为最后通讯作者) 。
王鹏飞/赵晓宇团队与成人动漫 孙蕾团队、香港大学朱轩团队等长期合作,先前(2024年10月)已于《自然通讯》(Nature Communications)上发表了题为“Lineage-specific pathogenicity, immune evasion, and virological features of SARS-CoV-2 BA.2.86/JN.1 and EG.5.1/HK.3”的研究,揭示了JN.1病毒如何迅速崛起成为全球主流毒株的机理。
近日,该团队又在Nature Communications发表两项最新研究:
一、SARS-CoV-2 KP.3.1.1如何通过积累关键突变位点获得竞争优势?
2025年12月11日,朱轩/王鹏飞/孙蕾/何茂洲/赵晓宇在《自然通讯》上发表研究成果——“Pathogenicity, virological features, and immune evasion of SARS-CoV-2 JN.1-derived variants including JN.1.7, KP.2, KP.3, and KP.3.1.1”。该研究不仅详细比较了不同SARS-CoV-2 JN.1子代病毒的病理学特征,并且深入探究了KP.3.1.1毒株如何通过关键突变位点获得竞争优势,从而成为2024年下半年的全球主流毒株的机制,为进一步理解冠状病毒致病性的分子机制以及冠状病毒演化过程提供了重要的实验依据。

继SARS-CoV-2 JN.1之后,其子代毒株相继出现并通过积累氨基酸突变获得传播优势,在这项研究中,研究者聚焦于包括JN.1.7,KP.2,KP.3和KP.3.1.1在内的关键毒株,尝试探究这些毒株获得优势的分子机制。通过比较其子代的基因组序列,研究者发现相较于相似度最高的KP.3毒株,KP.3.1.1毒株仅在刺突蛋白的S31位点和NSP10蛋白的S33位点携带氨基酸缺失或突变。研究者通过使用中和抗体、新冠病毒突破感染病人免疫血清和新冠病毒免疫仓鼠血清评估JN.1子代病毒的免疫逃逸能力,发现KP.3.1.1毒株的刺突蛋白具有最强的免疫逃逸能力。通过进一步的结构分析,证实S31位点缺失通过产生全新的N30位点糖基化修饰增强KP.3.1.1刺突蛋白的免疫逃逸能力。通过病毒转导实验,研究者证实携带有KP.3.1.1刺突蛋白的病毒相较于携带JN.1或KP.3刺突蛋白的病毒在细胞中的转导能力有十分显著的提升,凸显了S31位点缺失作为关键的免疫逃逸及感染能力双增强突变位点的重要价值!S31位点缺失显著增强了KP.3.1.1刺突蛋白的感染能力,但在复制实验中没有观察到KP.3.1.1复制能力的增强,进而研究者发现NSP10 S33C对平衡病毒复制能力和致病水平的重要作用。
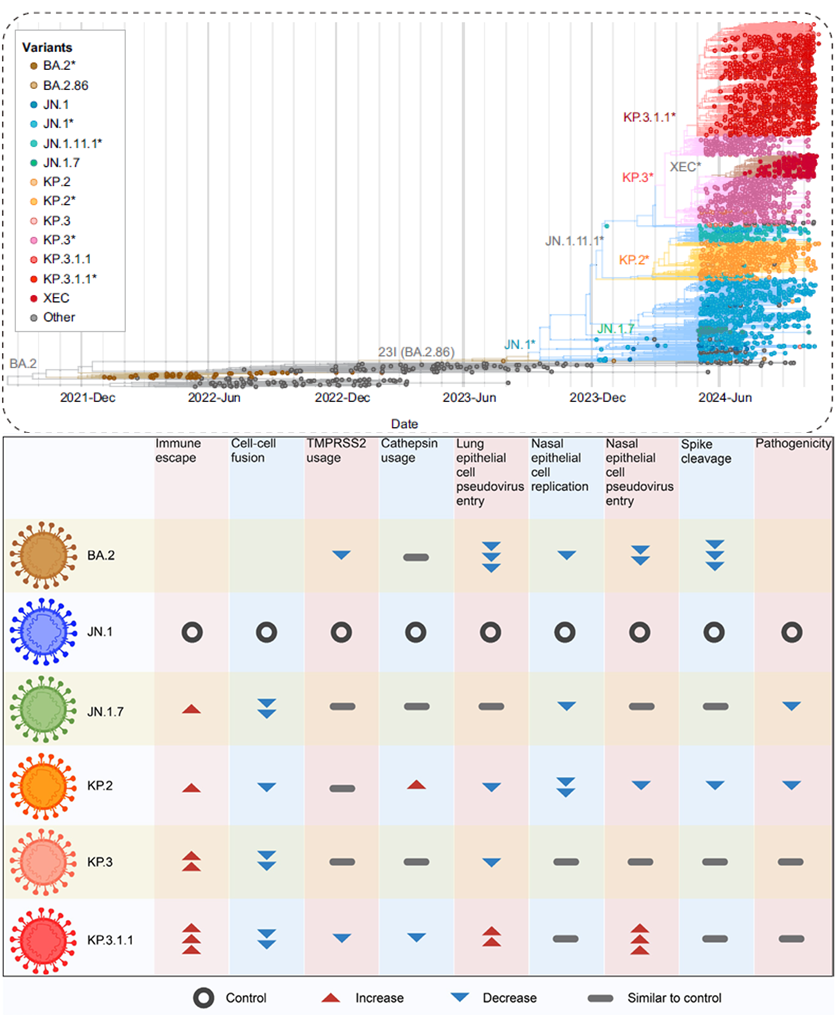
结合本研究的发现,研究者解释了SARS-CoV-2 KP.3.1.1通过积累关键氨基酸突变从而获得现有致病能力、免疫逃逸能力和基本病毒学特征,并成为世界主流毒株的分子机制。研究强调了刺突蛋白中免疫逃逸及感染能力双增强突变的重要价值,以及病毒通过刺突蛋白内外氨基酸突变共同塑造病毒总体特性的复杂机制。
香港大学史佳璐/成人动漫 赵晓宇青年研究员/成人动漫 金晓辉/成人动漫 李嘉言/香港大学刘妧晨/香港大学刘欢/贝湾生物科技有限公司胡叶凡博士为该成果的第一作者。香港大学朱轩教授、成人动漫 王鹏飞教授、成人动漫 孙蕾教授、国科大杭州高等研究院何茂州教授、成人动漫 赵晓宇青年研究员为该文章的共同通讯作者。
文章链接:
//www.nature.com/articles/s41467-025-66018-x
二、鉴定冠状病毒广谱中和抗体关键靶点
针对病毒复杂又高频的变异,发现保守表位开发高效广谱中和抗体十分关键。先前(2025年3月),王鹏飞/孙蕾/朱轩等团队在《Communications Biology》上发表两个具有广谱强效中和活性的抗体CYFN1006-1和CYFN1006-2,对包括新冠变异株KP.3.1.1及SARS-CoV-1在内的多种冠状病毒均表现出强效中和活性。
2025年11月26日,王乔/朱轩/王鹏飞/孙蕾等在《自然通讯》发表了另一项成果——“Orphan broadly RBD-binding antibodies annotate three remaining conserved RBD epitopes along SARS-CoV-2 evolution”。该研究首次通过创新的单B细胞筛选策略,从自然感染及突破感染人群中鉴定出稀有但极具价值的广谱抗体,这些抗体可跨谱系识别SARS-CoV-1、EG.5.1、BA.2.86、JN.1、KP.2/3等多种新冠新兴变异株,并在动物模型中展现真实保护效果。进一步的高分辨率结构分析显示,这些孤儿抗体精准靶向RBD上三个高度保守且互不重叠的关键表位,而且这些区域在全球数千万病毒序列中几乎未发生突变,构成病毒难以改变的“结构要害”。该研究表明,这三大表位是病毒最难逃逸的核心弱点,为广谱抗体药物与下一代疫苗开发提供黄金靶点,也为应对未来新变异株提供重要战略方向;随着病毒持续演化,抓住其“不可变的弱点”将成为未来免疫干预的关键路径。

文章链接:
//www.nature.com/articles/s41467-025-65596-0
王鹏飞课题组长期招聘博士后,有意者请将应聘材料通过电子邮件发至[email protected]邮箱。

